Την πρώτη από του στόματος θεραπεία για τη σοβαρή γυροειδή αλωπεκία ενέκρινε τη Δευτέρα ο Οργανισμός Τροφίμων και Φαρμάκων (FDA) των ΗΠΑ. Πρόκειται για τον εκλεκτικό και αναστρέψιμο αναστολέα της JAK1 και της JAK2, μπαρισιτινίμπη (baricitinib), που έχει ήδη θεραπευτική ένδειξη για άλλες δύο παθήσεις, τη ρευματοειδή αρθρίτιδα και την ατοπική δερματίτιδα.
Η αδειοδότηση του FDA για τη θεραπεία της σοβαρής γυροειδούς αλωπεκίας (που μόνο στις ΗΠΑ αφορά περισσότερα από 300.000 άτομα) κάνει την μπαρισιτινίμπη, την πρώτη φαρμακευτική αγωγή σε μορφή δισκίων που αντιμετωπίζει το πρόβλημα της απώλειας τριχοφυΐας όχι μόνο στο κρανίο αλλά σε όλο το σώμα.
Η γυροειδής αλωπεκία, που συνήθως αναφέρεται απλώς ως αλωπεκία, είναι μια αυτοάνοση διαταραχή κατά την οποία το σώμα επιτίθεται στους θύλακες της τρίχας, προκαλώντας την πτώση των μαλλιών, συχνά σε συστάδες. Η μπαρισιτινίμπη αναστέλλει τη δραστηριότητα μιας ή περισσότερων από μια συγκεκριμένη οικογένεια ενζύμων, παρεμβαίνοντας στην οδό που οδηγεί στη φλεγμονή.
«Η απόφαση έρχεται να καλύψει μια σημαντική ανεκπλήρωτη ανάγκη των ασθενών με σοβαρή γυροειδή αλωπεκία», ανέφερε η Kendall Marcus, Διευθύντρια του Τμήματος Δερματολογίας και Οδοντιατρικής στο Κέντρο Φαρμακευτικής Έρευνας και Αξιολόγησης του FDA.
Τι έδειξαν οι κλινικές μελέτες
Η απόφαση του αμερικανικού ρυθμιστικού φορέα βασίστηκε σε κλινικά δεδομένα δύο τυχαιοποιημένων, διπλών-τυφλών, placebo-ελεγχόμενων ερευνών (Trial AA-1 και Trial AA-2), στις οποίες είχαν λάβει μέρος ασθενείς με τουλάχιστον 50% απώλεια τριχοφυΐας κεφαλής για διάστημα μεγαλύτερο των έξι μηνών.
Οι συμμετέχοντες έλαβαν μια από τις ακόλουθες θεραπευτικές επιλογές: εικονικό σκεύασμα (placebo), 2 mg μπαρισιτινίμπη ή 4 mg μπαρισιτινίμπη σε καθημερινή βάση. Το πρωτεύον καταληκτικό σημείο και των δύο μελετών ήταν το ποσοστό των ασθενών που πετύχαν τουλάχιστον 80% κάλυψη της κεφαλής με τριχοφυΐα την 36η εβδομάδα.
Στην Trial AA-1 το 22% των 184 ασθενών που πήραν 2 mg μπαρισιτινίμπης και το 35% των 281 ασθενών που πήραν 4 mg μπαρισιτινίμπη πέτυχαν επαρκή κάλυψη του κρανίου με τριχοφυΐα, συγκριτικά με το 5% των 189 ασθενών που πήραν εικονικό φάρμακο. Στην Trial AA-2 το 17% των 156 ασθενών που πήραν 2 mg μπαρισιτινίμπη και το 32% των 234 ασθενών που πήραν 4 mg μπαρισιτινίμπη πέτυχαν επαρκή κάλυψη του κρανίου με τριχοφυΐα, συγκριτικά με το 3% των 156 ασθενών που πήραν placebo.
Οι συχνότερα αναφερόμενες ανεπιθύμητες ενέργειες που σχετίστηκαν με την μπαρισιτινίμπη ήταν: λοιμώξεις του ανώτερου αναπνευστικού, πονοκέφαλος, ακμή, υπερλιπιδαιμία, ουρολοιμώξεις, αύξηση της φωσφοκινάσης κρεατινίνης, αύξηση ηπατικών ενζύμων, θυλακίτιδα, κόπωση, λοιμώξεις του κατώτερου αναπνευστικού, ναυτία, αναιμία, μυκητιάσεις γεννητικών οργάνων, ουδετεροπενία, κοιλιακό άλγος, έρπης ζωστήρας και αύξηση σωματικού βάρους.
Αξίζει να σημειωθεί ότι, η μπαρισιτινίμπη δεν συστήνεται για συνδυαστική χρήση με άλλους αναστολείς JAK, βιολογικούς ανοσοτροποποιητές, κυκλοσπορίνη ή άλλα πιθανά ανοσοκατασταλτικά. Επίσης συνιστάται η στενή παρακολούθηση των ασθενών για τυχόν σημάδια και συμπτώματα λοίμωξης κατά τη διάρκεια και μετά τη θεραπεία, η αξιολόγηση των ασθενών για ενεργή φυματίωση και λανθάνουσα φυματίωση πριν τη θεραπεία και πιθανή ιική επανενεργοποίηση. Επιπλέον, άλλες προειδοποιήσεις και προφυλάξεις περιλαμβάνουν τις αλλεργικές αντιδράσεις, τις γαστρεντερικές διατρήσεις και ανωμαλίες όπως χαμηλά επίπεδα λευκών και ερυθρών αιμοσφαιρίων, αυξήσεις ηπατικών ενζύμων και αυξήσεις λιπιδίων.
Τέλος η μπαρισιτινίμπη συνοδεύεται από προειδοποίηση για σοβαρές λοιμώξεις, θνησιμότητα, κακοήθεια, σοβαρά ανεπιθύμητα καρδιαγγειακά συμβάντα και θρόμβωση.
Έως και 100% επανέκφυση μαλλιών
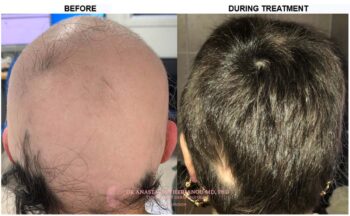
Σχολιάζοντας το ενθαρρυντικό αυτό νέο για όσους έχουν απώλεια τριχωτού κεφαλής λόγω γυροειδούς αλωπεκίας η Αναστασία Θεριανού, Διευθύντρια Δερματολογίας στο Imperial College NHS Trust εξηγεί στο ygeiamou.gr ότι «με τη χορήγηση του φαρμάκου αυτού μιλάμε για καλή ανταπόκριση με επανέκφυση των τριχών. Το φάρμακο αυτό ουσιαστικά μπλοκάρει την φλεγμονή γύρω από την ρίζα της τρίχας που έχει προκαλέσει την τριχόπτωση, με αποτέλεσμα οι τρίχες να επανεκφύονται έως και στο 100%».
Το πλεονέκτημα δε της μπαρισιτινίμπης έναντι άλλων διαθέσιμων θεραπειών είναι σύμφωνα με την κυρία Θεριανού ότι «καμία από τις έως τώρα διαθέσιμες θεραπείες δεν είναι εγκεκριμένη για χρήση της στην γυροειδή αλωπεκία. Αυτό βέβαια δεν σημαίνει ότι δεν είναι αποτελεσματικές ή είναι επικίνδυνες. Στην Δερματολογία πολύ συχνά χρησιμοποιούμε φάρμακα που ναι μεν είναι εγκεκριμένα για άλλες παθήσεις αλλά όχι για την καθ’ εαυτή πάθηση που το χρησιμοποιούμε. Επιπλέον οι έως τώρα θεραπείες δεν είναι αποτελεσματικές για όλους τους ασθενείς. Στην προκειμένη περίπτωση είναι υψίστης σημασίας το γεγονός ότι για πρώτη φορά εγκρίνεται ένα νέο φάρμακο για τις βαριές μορφές γυροειδούς αλωπεκίας, γιατί έχουμε ένα επιπλέον όπλο έναντι της πάθησης αυτής από την μία, αλλά επιστημονικά μας βοηθά να κατανοήσουμε καλύτερα σε βάθος τον μηχανισμό της πάθησης ώστε ενδεχομένως να βρεθούν νέα φάρμακα στο μέλλον».
Αναφορικά με τη διαθεσιμότητα της μπαρισιτινίμπης, όπως προαναφέρθηκε είναι ήδη διαθέσιμη στην Ελλάδα καθώς έχει λάβει ένδειξη για την ρευματοειδή αρθρίτιδα και σύντομα θα εγκριθεί και η χρήση του για τις σοβαρές μορφές ατοπικής δερματίτιδας. «Σύμφωνα με τις τελευταίες πληροφορίες που έχω, το φάρμακο θα εγκριθεί απο τον ευρωπαϊκό φορέα μέσα σε ένα μήνα, όποτε ευελπιστώ να είναι διαθέσιμο και στην Ελλάδα σε πολύ μικρό χρονικό διάστημα. Πρόκειται για ένα σκεύασμα υψηλού κόστους και πιστεύω ότι γι’ αυτό το λόγο η χορήγηση θα γίνεται από νοσοκομειακό φορέα και στην περίπτωση της γυροειδούς αλωπεκίας. Ωστόσο στην Μεγάλη Βρετανία που εργάζομαι, οι ασθενείς μπορούν να έχουν πρόσβαση σε αυτό μέσω ιδιωτικού φορέα. Το κόστος παραμένει υψηλό και στο Ηνωμένο Βασίλειο» καταλήγει η κυρία Αναστασία Θεριανού.






